Нитросоединения алифатические общая характеристика |
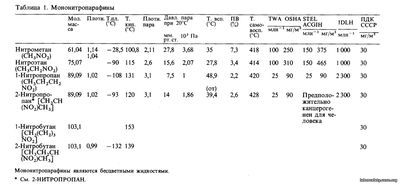
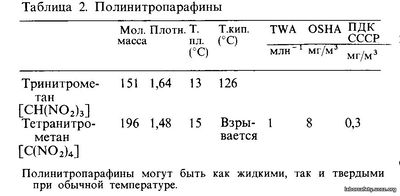
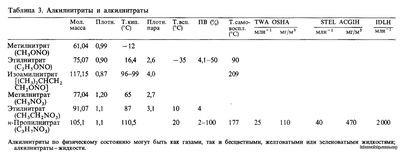
Нитросоединения характеризуются наличием химической связи —С—N02. К ним относятся мононитропарафины, полинитропарафины, нитроолефины, а также алкилнитриты и алкилнитраты. Мононитропарафины Мононитропарафины, свойства которых приведены в табл. 1, получают прямым нитрованием соответствующих парафинов в газовой фазе. Эти соединения используют главным образом в качестве растворителей для эфиров целлюлозы, других смол, а также для масел, жиров, воска и красителей. Среди мононитропарафинов выделяют группу хлорнитропарафинов. Другие наиболее важные мононитропарафины рассматриваются ниже. Нитрометан (CH3N02) - очень хорошо растворим в этиловом спирте, диэтиловом эфире и в меньшей степени - в воде маслянистая жидкость. Нитрометан получают разделением смеси нитрометана, нитроэтана и нитропропанов, образующейся при нитровании пропана. Кроме того, нитрометан получают при обработке метана оксидами азота под давлением. При обычных условиях нитрометан относительно стабилен, но при ударах или при нагревании он может взрываться. Разрушения, вызванные взрывом автоцистерн с нитрометаном, весьма значительны, поэтому рекомендуется хранить и транспортировать нитрометан расфасованным в малых емкостях - железных бочках. Вдыхание паров нитрометана вызывает эффект слабого раздражения, но возможно и отравление задолго до проявления наркотического действия; результатом повторяющегося воздействия может явиться поражение печени. Работать с нитрометаном нужно в условиях хорошей вентиляции, желательно местной вытяжной; следует использовать средства индивидуальной защиты. Нитроэтан (CH3CH2N02) - очень хорошо растворим в этиловом спирте и диэтиловом эфире; незначительно растворим в воде маслянистая жидкость с приятным запахом. Полинитропарафины Нитроолефины Нитроолефины могут быть получены дегидрированием Р-нитроспиртов или непосредственным присоединением оксидов азота к олефинам. Эти нитроолефины не имеют широкого промышленного применения. Алкилнитриты и алкилнитраты Алкилнитриты получают действием нитритов на спирты в присутствии разбавленной серной кислоты либо одновременно с мононитропарафинами при взаимодействии алкилгалогенидов с нитритами. Алкилнитриты используют главным образом в промышленных целях, кроме того, их применяют в органическом синтезе, в медицине в качестве терапевтических средств (сосудорасширяющие препараты). Они легко вступают в реакцию гидролиза с выделением азотистой кислоты, а также в реакции обмена при растворении в спиртах. Алкилнитраты получают в результате взаимодействия спиртов с азотной кислотой. Этилнитрат и в некоторой степени метилнитрат используют в органическом синтезе как нитрующий агент для ароматических соединений. Метилнитрат применяют и как ракетное топливо. Этилнитрат (CH3CH20N02) Этилнитрат получают этерификацией этилового спирта азотной кислотой или нитрующей смесью. Этилнитрат - легко воспламеняющаяся жидкость; при нормальных рабочих температурах в воздухе создаются взрывоопасные концентрации его паров. При нагревании этилнитрат может разлагаться со взрывом. Это вещество нельзя располагать вблизи источников воспламенения, за исключением тех случаев, когда этилнитрат используют в качестве топлива. Необходимо принять меры, предупреждающие случайные утечки жидкости из контейнера. Этилнитрат нельзя хранить в плохо вентилируемых помещениях. н-Пропилнитрат (CH3CH2CH2ONO2) растворим в этиловом спирте и диэтиловом эфире светло-желтая жидкость со сладковатым запахом. |
|
|

|

|